人類能認知到水分子的結構,依賴於科學的實驗方法論。
 結構決定空能,理解水分子的結構是關鍵
結構決定空能,理解水分子的結構是關鍵水,化學式為H2O,是由氫、氧兩種元素組成的無機物,無毒,可飲用。在常溫常壓下為無色無味的透明液體,被稱為人類生命的源泉。水是地球上最常見的物質之一,是包括無機化合、人類在內所有生命生存的重要資源,也是生物體最重要的組成部分。儘管水的行為複雜又獨特,它卻是又小又簡單的分子。它由兩個氫原子分別和一個氧原子鍵合而成。水分子的三個原子形成104.5度角。每個氫原子和氧原子之間的鍵,叫共價鍵,通過分享一對電子形成。應當指出,一對電子的共享程度並不均衡。氧比氫更需要電子(這種特性稱為電負性)。換言之,氫原子和氧原子鍵合時,在這個過程中共價電子主要在負電的氧原子周圍運動。因此,共價鍵氧的一側帶負電(-),氫的一側帶正電(+)。
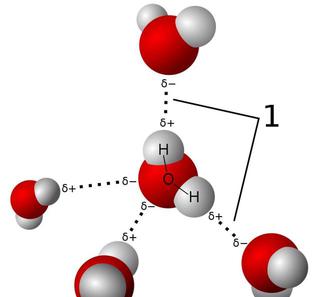 共價鍵的本質是共用電子
共價鍵的本質是共用電子為了檢驗正電荷均勻地分布在負電荷周圍,作用相互抵消。只有一個電荷中心;分子為無極性分子。但是水分子為非線性,呈角分布,因而差異很大。因為呈角分布,因而分子不對稱。在負電荷周圍,正電荷不均勻分布。作用不能相互抵消,兩者都有自己的電荷中心。分子有正負極。這是有極分子,化學家稱為偶極子。事實上,水分子是一種特殊的有極分子,其有極屬性比幾乎其他所有分子都明顯。水分子因而水分子呈非線性,且呈角分布。這方面哪怕稍有差池,生命就不會存在。因為偶極子有正極與負極,活像小磁鐵。
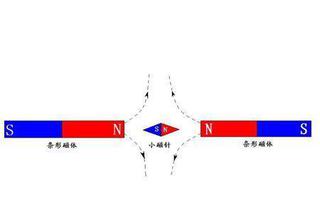 分子極不極性就看電荷分布是否對稱
分子極不極性就看電荷分布是否對稱分子的正極吸引鄰近分子的負極,從而分子黏在一起。水分子因其有明顯的偶極子屬件而由穩固的氫鍵結合在一起。它們趨於牢牢地粘在一起。牢固到什麼程度?用一個醫藥用的滴管,將水滴小心地滴到硬幣上。在水尚未從硬幣邊沿溢下來之前,數一下硬幣上的水滴數。水分子為了用別的方法演示水分子的黏性,在兩個玻璃杯或茶杯中分別裝上油和水,儘量將它們放平,分別在兩種液體上輕輕地放一個用密度比水和油大得多的鋼製成的小紙夾。紙夾本應沉入液體中,但事實是它漂浮在水面上,而不是在油上浮著。其實,紙夾浮在水面上並非因為有浮力,或兩者存在密度差異,而是因為水有黏性,水面上的分子粘在一起構成透不過去的覆蓋層,叫表面張力。
 表面張力的本質是一種電磁力
表面張力的本質是一種電磁力將紙夾往水面下壓,紙夾就會沉下去。黏在一起的分子形成固體和液體。為了使分子不黏在一起而相互分開,並變成氣體,必須向水中增加大量的能量,通常都通過加熱。就是說,水的沸點高,往往呈液態。必須將水溫提高到100℃,分子才能有足夠能量克服氫鍵的電磁作用力而分開。溫度在0℃和100℃之間時,水為液體。世界上幾乎所有地區的水全年多半為液體。但是如果水不呈角分布,無極性,而不是有極性,就不會很黏,水的沸點將特別低。
 所有物質的都受力場影響,沸點不是定值
所有物質的都受力場影響,沸點不是定值如果水無極性,估計在-65℃就會沸騰,那麼在地球的所有溫度下水都應該是氣體。水分子微波爐之所以能烹調食物,是因為食物中含水。水是一種強偶極子。電學上的水是正、負極性很強的分子。微波像無線電波、光和X射線一樣是一種電磁輻射能,具有電和磁兩種特性。電磁能穿過食物時,導致水等極化分子振動。振動產生熱,這種熱煮熟放在微波爐中的食物。微波爐並不是常說的由裡向外煮熟食物,煮熟食物的熱源來自食物內部而不是外部。水妙不可言,實際上是分子的妙不可言。實際上水是液體,水分子呈角分布且有極性,而不是呈線性分布且無極性,因此水成為生命的源泉。